Contenidos
- Ciclo Hidrologico .com
- Reservorios de agua y tiempos de residencia
- Procesos del agua
- Cambios temporales y efectos climáticos
- Precipitación
- Escorrentía superficial
- Infiltración del agua
- Evaporación
- Sublimación
- Advección
- Condensación
- Efectos sobre la civilización humana
- Efectos sobre la vida
- Hidrología
- Vídeos
- Bibliografía
Otros sitios
Evaporación
La evaporación es el proceso por el cual las moléculas en estado líquido (por ejemplo, el agua) se hacen gaseosas espontáneamente (ej.: vapor de agua). Es lo opuesto a la condensación. Generalmente, la evaporación puede verse por la desaparición gradual del líquido cuando se expone a un volumen significativo de gas. Por término medio, las moléculas no tienen bastante energía para escaparse del líquido, porque de lo contrario el líquido se convertiría en vapor rápidamente. Cuando las moléculas chocan, se transfieren la energía de una a otra en grados variantes según el modo en que chocan.
Los líquidos que no parecen evaporarse visiblemente a una temperatura dada en un gas determinado (p.ej., el aceite de cocina a temperatura ambiente) poseen moléculas que no tienden a transferirse la energía de una a otra como para darle "la velocidad de escape" (la energía calórica) necesaria para convertirse en vapor. Sin embargo, estos líquidos se evaporan, pero el proceso es mucho más lento y considerablemente menos visible.
La evaporación es una parte esencial del ciclo del agua. La energía solar provoca la evaporación del agua de los océanos, lagos, humedad del suelo y otras fuentes de agua. En hidrología, la evaporación y la transpiración (que implica la evaporación dentro del estoma de la planta) reciben el nombre conjunto de evapotranspiración.
Teoría cinética
Para que las moléculas de un líquido se evaporen, deben estar localizadas cerca de la superficie, moverse en la dirección apropiada y tener la energía cinética suficiente como para vencer las fuerzas intermoleculares de la fase líquida. Sólo una pequeña proporción de las moléculas cumplen con estos criterios, por lo que la tasa de evaporación es limitada.
Debido a que la energía cinética de una molécula es proporcional a su temperatura, la evaporación se produce más rápido conforme la temperatura es más alta. Como las moléculas que se mueven más rápido escapan, las moléculas restantes tienen una energía cinética media inferior, y por tanto la temperatura del líquido disminuye. Este fenómeno se conoce como refrigeración evaporativa, y es la razón por la cual la evaporación del sudor refresca el cuerpo humano.
La evaporación también tiende a producirse más rápidamente con tasas de flujo más altas entre la fase gaseosa y líquida, y en líquidos con presión de vapor más alta. Por ejemplo, la ropa tendida en un cordel secará (por evaporación) más rápidamente durante un día ventoso que en un día sin viento. Tres puntos claves de la evaporación son el calor, la humedad y el movimiento del aire.
Equilibrio evaporativo
Si la evaporación ocurre en un recipiente cerrado o en sitios calientes, las moléculas que se escapan se acumularán como vapor encima del líquido. Muchas de las moléculas vuelven al líquido, haciéndose el retorno más frecuente conforme la densidad y la presión del vapor aumentan. Cuando el proceso de fuga y retorno alcanza un equilibrio, se dice que el vapor está "saturado", y ya no se dará ningún cambio adicional en la presión o la densidad del vapor. Para un sistema que consiste en vapor y líquido de una sustancia pura, este estado de equilibrio está directamente relacionado con la presión de vapor de la sustancia, como viene expresado en la relación de Clausius-Clapeyron:
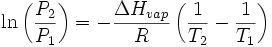
donde P1 y P2 son las presiones de vapor a temperaturas T1 y T2 respectivamente, ΔHvap es la entalpía de la vaporización, y R es la constante universal de los gases. La tasa de evaporación en un sistema abierto está relacionada con la presión de vapor encontrada en un sistema cerrado. Si un líquido se calienta, cuando la presión de vapor alcance la presión ambiental, el líquido hervirá.
La capacidad para evaporarse de la molécula de un líquido se debe en gran parte a la cantidad de energía cinética que una partícula individual pueda poseer. Incluso a temperaturas inferiores, las moléculas individuales de un líquido pueden evaporarse potencialmente si tienen más de la cantidad mínima de energía cinética requerida para la vaporización.
Factores que influyen en la tasa de evaporación
* Concentración de la sustancia que se evapora en el aire. Si el aire ya tiene una alta concentración de la sustancia que se evapora, entonces la sustancia se evaporará más despacio.
* Concentración de otras sustancias en el aire. Si el aire ya está saturado con otras sustancias, puede tener una capacidad inferior para la sustancia que se evapora.
* Tasa de flujo de aire. Si aire fresco se mueve sobre la sustancia todo el tiempo, la concentración de la sustancia en el aire tendrá menos probabilidad de subir con el tiempo, potenciando así una evaporación más rápida. Esto resulta en una capa divisoria en la superficie de evaporación que disminuye con la velocidad de flujo, disminuyendo la distancia de difusión en la capa estancada.
* Concentración de otras sustancias en el líquido (impurezas). Si el líquido contiene otras sustancias, tendrá una capacidad inferior para la evaporación.
* Temperatura de la sustancia. Si la sustancia está más caliente, la evaporación será más rápida.
* Fuerzas intermoleculares. Cuanto mayores son las fuerzas que mantienen las moléculas juntas en el líquido, más energía será necesaria para evaporarlas.
* Área superficial. Una sustancia que tiene un área superficial más grande se evaporará más rápido, ya que hay más moléculas superficiales que son capaces de escaparse.
* Calentamiento. Cuanto más grueso es el recipiente donde se está calentando, más se reduce la evaporación del agua, debido a que se dedica menos calor a los propia evaporación.
En los Estados Unidos, el Servicio Meteorológico Nacional mide la tasa actual de evaporación en "ollas" estandarizadas de agua abiertas al aire libre en varias localizaciones a escala nacional. Otros servicios hacen lo mismo alrededor del mundo. Los datos estadounidenses son compilados en un mapa de evaporación anual. Las medidas varían entre 30 y más de 120 pulgadas por año.
Aplicaciones
Secado
Cuando la ropa se cuelga de un cordel, aunque la temperatura ambiental esté por debajo del punto de ebullición del agua, el agua se evaporará. Este proceso se acelera por factores como humedad baja, calor (del sol) y viento. En un secador de ropa, se hace pasar aire caliente por las prendas, permitiendo que el agua se evapore muy rápidamente.
Combustión
Las gotitas de combustible se vaporizan, cuando reciben calor, mezclándose con los gases calientes en la cámara de combustión. El calor (energía) también puede ser recibido por radiación de cualquier pared refractaria caliente de la cámara de combustión.
Deposición de capas
Evaporando una sustancia y condensándola en un sustrato es posible depositar capas delgadas.